Воспаление. Экссудация. Экссудат и транссудат. Часть 5
Содержание статьи
Перенос жидкой части крови и белков из крови в ткани называется экссудацией, а сама жидкость называется экссудатом.
Механизм экссудации при воспалении
Воспалительная экссудация — сложный процесс, основными механизмами которого являются:
- повышенная проницаемость капилляров и венозных стенок;
- гиперосмия и в меньшей степени, гиперонхия в очаге воспаления;
- изменение фильтрации жидкости в капиллярах;
- нарушение лимфообращения.
Повышенная проницаемость капилляров и венозных стенок
Повышенная проницаемость является основным фактором патогенеза воспалительной экссудации. Существует две фазы увеличения проницаемости стенок кровеносных сосудов:
- Немедленное увеличение проницаемости, связанное с высвобождением транзиторных медиаторов;
- Позднее длительное (несколько часов) увеличение проницаемости из-за накопления нейтрофилов в очагах воспаления — высвобождение лизосомных ферментов, катионных белков, а также медиаторы пролонгированного действия.
Везикуляция
Электронно-микроскопические исследования показали, что экссудация направляется:
- через эндотелиальные щели;
- через эндотелиальные клетки через внутриклеточные канальцы;
- через пузырьки.
Под влиянием гистамина и серотонина сократительный белок (микрофибриллы) эндотелиальных клеток сжимается, и между этими клетками образуются поры и отверстия. Хинины и другие медиаторы вызывают образование мелких пузырей (пузырьков) в эндотелиальных клетках, а также отек под эндотелием.
Образование везикул и транспорт веществ через эндотелиальную клетку — так называемая везикуляция или ультрапиноцитоз — считается активным процессом, требующим энергии и тесно связанным с системами клеточных мембран аденилциклазы, гуанилциклазы, холинэстеразы и других ферментов.
![]() Везикуляция
Везикуляция
Изменение фильтрации жидкости в капиллярах
Также важны при экссудации изменения фильтрации жидкости в капиллярах.
В нормальных условиях, хотя гидростатическое давление крови снижается от артериального конца капилляра к венозному, оно превышает гидростатическое давление ткани, разница между этими давлениями составляет эффективное гидростатическое давление, которое облегчает перенос жидкости из капилляра в ткань.
Онкотическое (коллоидосмотическое) давление крови от конца капиллярной артерии к венозному практически не изменяется и превышает онкотическое давление тканей; разница между этими давлениями и есть эффективное онкотическое давление.
Онкотическое давление работает в отличие от гидростатического — оно удерживает жидкость в капилляре. Эффективное гидростатическое давление на артериальном конце капилляра больше, чем эффективное онкотическое давление, что приводит к ультрафильтрации жидкости из капилляра в ткани.
Напротив, из-за снижения гидростатического давления на венозном конце капилляра эффективное онкотическое давление выше, чем эффективное гидростатическое давление, и поэтому жидкость течет в противоположном направлении — от ткани в капилляре. Часть межклеточной жидкости возвращается в кровоток через лимфатическую систему.
По мере увеличения гидростатического давления крови (HtT) ультрафильтрация жидкости из капилляров в ткань естественным образом становится более интенсивной. В то же время увеличивается площадь стенки капилляра, через которую жидкость фильтруется в ткани. Это уменьшает площадь стенки капилляра, через которую жидкость течет обратно из тканей.
Это один из основных механизмов развития так называемого механического или застойного отека. Он играет важную роль в возникновении отеков у сердечных больных, беременных (отек ног), а также при тромбофлебите, воспалении и других случаях.
![]() Отек ног при беременности
Отек ног при беременности
При снижении онкотического давления крови, конечно, снижается и эффективное онкотическое давление, и развивается так называемый онкотический отек. Площадь стенки капилляра, через которую жидкость фильтруется в ткани, увеличивается. Площадь стенки капилляра, через которую жидкость возвращается в капилляр, уменьшается.
Наиболее выраженное увеличение площади фильтрации (OtD) и уменьшение площади возврата жидкости (DT) наблюдается при увеличении эффективного гидростатического давления (HtT) и одновременном снижении эффективного онкотического давления (OtT).
В условиях воспаления артериолы и прекапилляры расширяются, а количество функциональных артериол увеличивается. Повышение скорости кровообращения и гидростатического давления в капиллярах. Все это способствует экссудации. Однако нарушение притока крови к венозному концу капилляров имеет решающее значение для развития экссудации, поскольку препятствует возвращению жидкости в капилляры. Следовательно, экссудация возникает в основном на фоне венозной гиперемии.
Таким образом, воспалительному отеку способствует как повышение гидростатического давления в кровеносном сосуде (в основном, на венозном конце капилляра), так и повышение онкотического давления в тканях. Однако изменения онкотического давления менее важны для развития воспалительного отека, чем изменения осмотического давления.
Нарушение лимфообращения
Экссудация и воспалительный отек также играют важную роль в развитии лимфатических расстройств рефлюкса. Но постоянной связи между терминальными лимфатическими капиллярами и внесосудистыми межклеточными канальцами обнаружено не было.
Когда канальцы заполнены межклеточной жидкостью, они доставляют эту жидкость к капиллярам (жидкость поступает в капилляры через эндотелиальные отверстия). Затем канальцы схлопываются и отделяются от капилляров, в то время как эндотелиальные отверстия закрываются.
В случае воспаления эндотелий лимфатических капилляров повреждается, и внесосудистые канальцы выходят из эндотелиальных отверстий. Развивается так называемый динамический сбой лимфатической системы — лимфатическая система перестает выполнять функции оттока жидкости и развиваются отеки. Нарушения лимфодренажа возникают рано и сохраняются до конца воспаления.
Количество, состав, pH и содержание белка (альбумин, глобулин, фибриноген) в экссудате зависят от патогенных агентов (микроорганизмов, токсинов), вызывающих конкретное воспаление. В прошлом считалось, что по мере увеличения проницаемости сосудов эндотелий действует как простой фильтр — сначала из кровеносного сосуда покидают более мелкие молекулы (альбумины), затем глобулины и, наконец, фибриноген.
В настоящее время считается, что помимо степени увеличения проницаемости сосудов состав экссудата также определяется природой патогенного агента. Например, фибринозный экссудат с высоким содержанием фибриногена, но с низким содержанием глобулина и альбумина. Резорбция белка из экссудата также может играть роль. Если, например, альбумин больше резорбируется, количество глобулина в экссудате может увеличиться.
Экссудат и транссудат
Экссудат — это жидкость, образующаяся при воспалительных заболеваниях и часто инфицированная микроорганизмами.
Транссудат, с другой стороны, представляет собой жидкость, которая переместилась в атипичный участок тела без признаков воспаления, таких как отек или асцит.
![]() Асцит
Асцит
В клинике очень важно определить, является ли скопившаяся в той или иной области тела жидкость результатом воспаления, поэтому важно отличать экссудат от транссудата.
Типы и отличительные характеристики экссудата
Макроскопически экссудат, как и транссудат, может быть прозрачным, но также может быть опалесцирующим, желтовато-зеленым, гнойным и кровянистым. Между лабораторными тестами на экссудат и транссудат существует несколько существенных различий.
- Из-за повреждения клеток увеличивается активность гидролитических ферментов экссудата.
- Осмотическое давление экссудата превышает осмотическое давление транссудата.
Выделяют следующие основные типы экссудата:
- серозный;
- блютанговый;
- фибринозный;
- геморрагический;
- гнойный.
Серозный экссудат
Серозный экссудат наиболее близок к транссудату — это желтоватая, почти прозрачная жидкость с относительно невысокой относительной плотностью и содержанием кровяных телец. Таким экссудатом может быть ожог кожи II стадии, экссудативный плеврит, серозный менингит и другие случаи.
Блютанговый экссудат
В экссудате блютанга, помимо компонентов серозного экссудата, присутствует слизь. Это происходит в случаях воспаления слизистых оболочек (дыхательных путей, желудочно-кишечного тракта), таких как ринит (воспаление слизистой оболочки носа) и колит (воспаление слизистой оболочки толстой кишки).
Фибринозный экссудат
Фибринозный экссудат возникает, когда фибриноген выходит из кровеносных сосудов и переходит в ткани, где он превращается в фибрин. Фибринозный экссудат также образуется на серозных оболочках и слизистых оболочках из-за пневмококков, дифтерии, дизентерийных палочек и других микробов.
Существует два типа фибринозного экссудата — крупозный и дифтерийный экссудат.
- Крупный экссудат, например, у больных с тяжелой пневмонией, обнаруживается в виде пленки на слизистой оболочке альвеол легких. Удаление этой пленки не повредит слизистые оболочки.
- Дифтерийный экссудат проникает через слизистую оболочку и вызывает некроботические изменения. После удаления дифтерийного экссудата язва остается.
По мере развития воспаления фибриновые пленки растворяются фибринолитической системой.
Геморрагический экссудат
Геморрагический экссудат возникает в результате сильного повреждения стенок кровеносных сосудов, когда в экссудат попадают эритроциты. Обычно это происходит, когда воспаление очень быстрое. Геморрагический экссудат измеряется у пациентов с перитонеальной, плевральной и перикардиальной полостями, пустулами черной оспы, обморожением II степени, аллергическим воспалением (феномен Артуса).
![]() Геморрагический экссудат
Геморрагический экссудат
Гнойный экссудат
Гнойный экссудат образуется в результате действия гнойных микроорганизмов (стрептококков, стафилококков, туберкулезных палочек). Этот экссудат богат клетками, в основном лейкоцитами. Если острое гнойное воспаление вызвано стрептококками или стафилококками, нейтрофилы преобладают в экссудате, но если воспаление и экссудация вызваны, например, паразитами животных, количество эозинофилов в экссудате увеличивается.
Гнойный экссудат представляет собой вязкую жидкость желтовато-зеленого цвета с характерным сладким запахом. При центрифугировании он распадается на два слоя — сывороточный и клеточный осадок. Гнойные клетки — так называемые гнойные тельца — это поврежденные и мертвые клетки крови (нейтрофилы, лимфоциты, моноциты), клетки воспаленной ткани и микроорганизмы.
В цитоплазме гноя много вакуолей, граница гноя с окружающей средой нечеткая. Наблюдается также кариолиз — набухание и постепенное растворение ядра гноя, в результате чего количество нуклеотидов и нуклеиновых кислот в гное увеличивается. Гнойная сыворотка химически существенно не отличается от сыворотки крови.
- Гнойный экссудат туберкулезного и сифилитического воспаления обычно имеет большое количество лимфоцитов.
- Гнойный экссудат опухоли содержит множество опухолевых клеток и эритроцитов.
Относительная плотность гнойного экссудата высокая (1020-1040). В нем много активных ферментов, продуктов интенсивного протеолиза (полипептиды, аминокислоты), молочная кислота (90-120 мг% и более). Из-за интенсивного гликолиза содержание глюкозы в гнойном экссудате, как и в других экссудатах, обычно ниже, чем в крови (40-50 мг%).
На практике распространены сочетания различных типов воспалений, таких как серозный фибриноз, гнойный фибриноз, геморрагический гнойный экссудат. Заражение любого вида экссудата гнилостными микробами приводит к гниению экссудата.
Капли жира (hilozo) также могут попадать во все экссудаты и создавать так называемый хилозо-экссудат. Этот экссудат возникает, например, когда воспаление локализовано в брюшной полости, области больших лимфатических сосудов.
Продолжение статьи
- Часть 1. Этиология и патогенез воспаления. Классификация.
- Часть 2. Особенности обмена веществ при воспалении.
- Часть 3. Физико — химические изменения. Роль нервной и эндокринной систем в развитии воспаления.
- Часть 4. Изменения в периферическом кровообращении при воспалении.
- Часть 5. Экссудация. Экссудат и транссудат.
- Часть 6. Эмиграция лейкоцитов. Хемотаксис.
- Часть 7. Фагоцитоз. Асептическое и острое воспаление.
- Часть 8. Распространение. Последствия. Принципы лечения воспаления.
Источник
Расстройства кровообращения и микроциркуляции при воспалении
Стадии расстройства микроциркуляции:
1. Кратковременный спазм артериол:результат рефлекторного возбуждения вазоконстрикторов на воздействие флогогена (несколько сек-мин).
2. Артериальная гиперемия:увеличение притока артериальной крови и кровенаполнения ткани. Способствует усилению оксигенации тканей, снижению степени ацидоза, активации обмена веществ.
3. Венозная гиперемия:сопровождается замедлением тока крови, расширением просвета посткапилляров и венул. В механизме выделяют 3 группы факторов:
нарушения реологических свойств крови;
изменения сосудистой стенки;
тканевые изменения.
4. Предстаз:периодические маятникообразные движения крови «вперёд ↔ назад» в результате механического препятствия оттоку крови по посткапиллярам, венулам и венам агрегатами форменных элементов крови в просвете сосуда и пристеночными микротромбами.
5. Стаз:возникает в результате закрытия просвета микрососудов агрегатами клеток изнутри и сдавления экссудатом снаружи. Является завершающей стадией сосудистых изменений.
Экссудация
Экссудация (от лат.exsudatio- выпотевание) — компонент воспаления, включающий в себя триаду: сосудистые реакции и изменения кровообращения в очаге воспаления; выход жидкой части крови из сосуда (собственно экссудацию); эмиграцию (выход лейкоцитов в очаг воспаления и развитие фагоцитарной реакции).
Основная причинаэкссудации — увеличение проницаемости стенок микрососудов вследствие множества процессов, повреждающих их стенку.
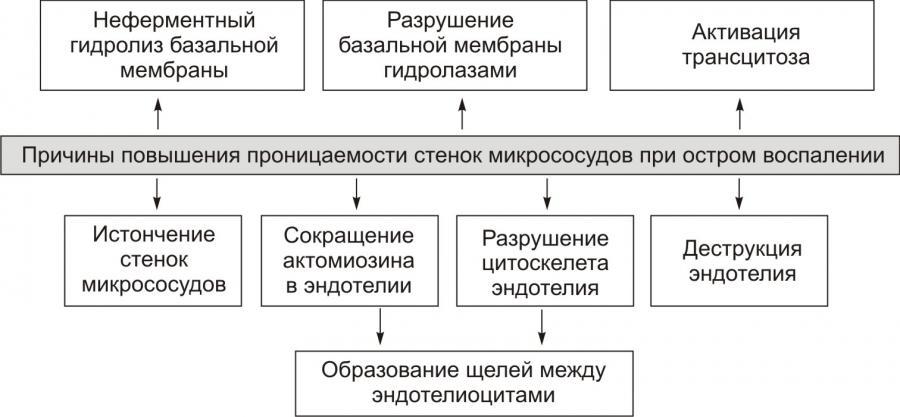
Рис. 9. — Причины повышения проницаемости стенок микрососудов
при остром воспалении (по П.Ф. Литвицкому, 2002)
Основные факторы механизма экссудации:
1) повышение проницаемости сосудов (венул и капилляров) в результате воздействия медиаторов воспаления и в ряде случаев самого воспалительного агента — ведущий фактор;
2) увеличение кровяного (фильтрационного) давления в сосудах очага воспаления вследствие гиперемии;
3) возрастание осмотического и онкотического давления в воспаленной ткани в результате альтерации и начавшейся экссудации и, возможно, снижение онкотического давления крови из-за потери белков при обильной экссудации.
Виды экссудата
1. Серозный экссудат: состоит из полупрозрачной жидкости, богатой белком (до 2-3%), и немногочисленных клеток, в том числе форменных элементов крови (ФЭК).
2. Фибринозный экссудат: содержит большое количество фибриногена и фибрина.
3. Гнойный экссудат:мутная густая жидкость, содержащая до 6-8% белка и большое количество различных форм лейкоцитов, микроорганизмов, погибших клеток повреждённой ткани.
4. Геморрагический экссудат:содержит большое количество белка и эритроцитов, а также другие ФЭК.
5. Гнилостный (ихорозный) экссудат: любой вид экссудата может приобрести гнилостный (ихорозный) характер при внедрении в очаг воспаления гнилостной микрофлоры (анаэробы).
6. Смешанные формыэкссудата могут быть самыми разнообразными (например, серозно-фибринозный, гнойно-фибринозный, гнойно-геморрагический и др.).
Значение процесса экссудации в очаге воспаления
Адаптивное:
транспорт медиаторов воспаления
доставка иммуноглобулинов в очаг воспаления
удаление из крови метаболитов и токсинов
задержка и/или фиксация в очаге воспаления флогогена и продуктов его действия на ткань
Патогенное:
сдавление, смещение органов и тканей экссудатом
возможность излияния экссудата в полости тела и сосуды
формирование абсцессов, развитие флегмон
Эмиграция (emigratio, от лат.emigrare — выселяться, переселяться) — выход лейкоцитов из сосудов в ткань.Осуществляется путем диапедеза через стенку венул и является ключевым событием патогенеза воспаления.
Стадии процесса эмиграции лейкоцитов в очаге воспаления:
1. краевое стояние лейкоцитов;
2. адгезия к эндотелию и проникновения через сосудистую стенку;
3. направленное движение лейкоцитов в очаге воспаления.
На стадии краевого стояния(маргинации) условно выделено четыре последовательных этапа.
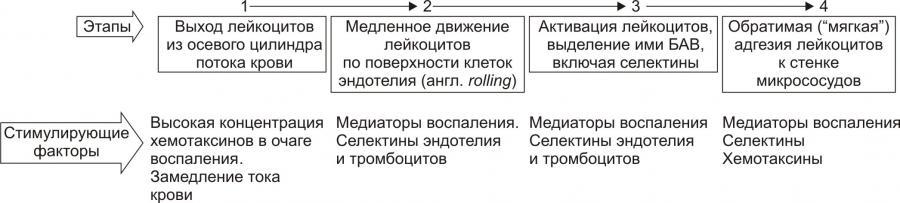
Рис. 10. -Этапы стадии краевого стояния лейкоцитов и факторы, стимулирующие краевое стояние (по П.Ф. Литвицкому, 2002)
В стадии адгезии и выхода лейкоцитов выделяют 2 этапа: устойчивой («плотной») адгезии (1) и прохождения лейкоцитов через стенку микрососуда (2).

Рис. 11. -Этапы стадии устойчивой адгезии и прохождения лейкоцитов через стенку микрососуда; факторы, стимулирующие адгезию (по П.Ф. Литвицкому, 2002)
Значение эмиграции лейкоцитов в очаг воспаления:
поглощение и деструкция флогогенного фактора;
поглощение и деструкция поврежденных клеток и неклеточных структур;
синтез и выделение медиаторов воспаления;
поглощение и «процессинг» антигенов и презентация последних лимфоцитам;
развитие иммунных и/или аллергических реакций.
Источник
13. Экссудация. Механизмы развития воспалительного отека.
Экссудация — выход жидкой части крови, электролитов, белков и клеток из сосудов в ткани.
Механизмы экссудации:
повышение проницаемости сосудистой стенки под влиянием медиаторов воспаления;
повышение внутрисосудистого гидростатического давления в связи с изменениями кровообращения в очаге воспаления;
повышение онкотического давления из-за увеличения содержания белка вне сосудистой стенки;
уменьшение внутрисосудистого онкотического давления в связи с потерей белка вместе с экссудатом;
повышение коллоидно-осмотического давления ткани в зоне альтерации;
активация цитокемсиса, когда эндотелиальные клетки начинают пропускать через себя плазму клетки и растворимые в ней соединения.
Фазы экссудации:
ранняя фаза экссудации возникает через 10-15 минут с момента действия альтернирующего фактора и достигает максимума через 30 минут. Обусловлена выбросом гистамина, серотонина, активаций калликреин-кининовой системы, системы комплимента;
поздняя фаза экссудации начинается чуть позже, достигает максимума через 4-7 часов. Может быстро свернуться, а может длиться до 3-4 суток. Обусловлены образованием эйкозаноидов, выбросом монолимфокинов, свободных радикалов, биологически активных веществ нейтрофилов.
Виды экссудата:
серозный. Близок по составу к транссудату, содержит альбумины, образуется в серозных полостях;
геморрагический — содержит эритроциты в большом количестве. Характерен для септических состояний, стафилококковой инфекции;
фибринозный;
гнойный — содержит лейкоциты, вызван распадом клеток;
гнилостный;
смешанный.
Функции экссудата — в результате экссудации происходит разбавление концентрации бактериальных и других токсинов и разрушение их поступающими из плазмы крови протеолитическими ферментами. В ходе экссудации в очаг воспаления поступают сывороточные антитела, которые нейтрализуют бактериальные токсины и опсонизируют бактерии. Воспалительная гиперемия обеспечивает переход в очаг воспаления лейкоцитов крови, способствует фагоцитозу. Фибриноген экссудата превращается в фибрин, нити которого создают структуру, облегчающую переход лейкоцитов в рану. Фибрин играет важную роль в процессе заживления ран.
Однако экссудация имеет и отрицательные последствия — отек тканей может привести к удушью или угрожающему для жизни повышению внутричерепного давления. Нарушения микроциркуляции способны привести к ишемическому повреждению тканей. Излишнее отложение фибрина может препятствовать последующему восстановлению поврежденной ткани и способствовать избыточному разрастанию соединительной ткани. Поэтому врач должен осуществлять эффективный контроль за развитием экссудации.
14. Механизмы и биологическое значение эмиграции лейкоцитов
Эмиграция — выход лейкоцитов за пределы сосудистого русла в зону альтерации.
Осуществляется путем проникновения через сосудистую стенку. В эмиграции лейкоцитов в очаг воспаления наблюдается определенная очередность: сначала эмигрируют нейтрофильные гранулоциты, затем моноциты, позже лимфоциты.
Эту последовательность впервые описал И. И. Мечников. Более позднее проникновение моноцитов объясняется их меньшей хемотоксической чувствительностью.
Эмиграция нейтрофилов начинается через 10-12 минут, достигает максимума через 3-4 часа. При острых воспалительных процессах в зоне воспаления преобладают нейтрофилы (до 95 %). Миграция моноцитов начинается через 16-18 часов, массовая — в течение 3-4 суток.
Лимфоциты эмигрируют спустя сутки и преобладают в зоне хронического воспалительного процесса.
Механизмы эмиграции:
А) действие хемотропных веществ. В очаге воспаления осуществляется активное движение лейкоцитов и к химическим раздражителям. Это явление описал И.И. Мечников и назвал его хемотаксис.
Хемотропные вещества: продукты жизнедеятелности микроорганизмов, продукты протеолиза тканей, продукты нибринолиза.
Компоненты комплемента С3 и С5, компоненты калликреин-кининовой системы, лимфокины, лейкотриены.
Хемоатрактанты взаимодействуют со специфическими рецепторами на мембране лейкоцитов. Возникает метаболический взрыв, образуются свободные радикалы. Мембрана начинает синтезировать адгезивные гликопротеины, понижается поверхностное натяжение мембраны и создаются условия для формирования псевдоподий. Одновременно возникает активация актино-миозиновых комплексов, что ведет к сократительному акту, и клетка передвигается в зону образования псевдоподий.
Поглощение объекта лейкоцитами может происходить двумя способами: контактирующий с объектом участок цитоплазмы втягивается внутрь клетки, а вместе с ним втягивается и объект. Второй способ заключается в том, что фагоцит прилагается к объекту своими псевдоподиями, а потом всем телом подтягивает в сторону объекта и обволакивает его. В итоге образуется фагосома, к которой приближается лизосома и начинается переваривание под действием лизосомальных ферментов;
Б) развитие тромбоза, эмболии, изменение реологических свойств крови: повышение вязкости и снижение скорости кровотока;
В) повышение адгезивности эндотелиальных клеток;
Г) повышение проницаемости сосудистой стенки под влиянием биологически активных веществ, медиаторов воспаления, лизосомальных ферментов;
Д) действие электроэнергетических сил.
В зоне альтерации нормируется положительный потенциал за счет избыточного накопления Н+, а лейкоциты на своей поверхности несут суммарный отрицательный Z-потенциал.
Соседние файлы в папке К экзамену
- #
- #
- #
- #
- #
- #
Источник